Al Oh 3 Hno3 EDUCA

1 ответ. Xumuk ответил 7 лет назад. В результате взаимодействия гидроксида калия с гидроксидом алюминия, проявляющим амфотерные свойства, из-за чего эта реакция и становится возможной (Al (OH)3 + KOH.
Запишите молекулярное и ионное уравнения реакции. помогите пожалуйстааа 1) hno3 + al(oh)3 = 2

Решенное и коэффициентами уравнение реакции Al2(SO4)3 + 6 NaOH → 2 Al(OH)3 + 3 Na2SO4 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
How to Balance NaOH + Al = Al(OH)3 + Na (Sodium Hydroxide and Aluminum) YouTube

Al(OH)3 + NaOH + 2H2O = Na[Al(H2O)2(OH)4] - молекулярное уравнение. Na Al O 2 + 2 H 2 O =Na[Al(OH)4] Ионное уравнение.
Составить ионные уравнения AlCl3+6NaOH=Al(OH)3 Al(OH)3+3HCl=AlCl3+3H2O Al(OH)3+NaOH=Na [Al(OH)4

Лучший ответ. Штирлиц Высший разум (318206) 12 лет назад. Al (3+) + 3NO3- + 3Na+ + 3OH- = Al (OH)3 + 3Na+ + 3NO3-. Al (3+) + 3OH- = Al (OH)3. Остальные ответы. Похожие вопросы. Пользователь Артём Катков задал вопрос в категории.
[Solved] Acidbase reaction Al(OH)₃ + NaOH 9to5Science
Решенное и коэффициентами уравнение реакции Al(OH)3 + NaOH → Na[Al(OH)4] с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
Сума коефіцієнтів яка? K2o+h2o =naoh Al(oh)3=al2o3+h2o Na+h20=naoh+h2 C2h4+02=co2+h20 Школьные

Ответы на вопрос Помогите решить al(oh)3 + naoh. Что влияет на результат реакции гидроксида алюминия и гидроксида? Задача: сколько соли образуется при сплавлении 90 г NaOH и 80 г Al(OH)3. Какого вещества в избытке.
BalanceAl(OH)3 + NaNO3 = Al (NO3)3 + NaOH Please Show the Solution because I'm not really good

Решенное и коэффициентами уравнение реакции 3 NaOH + Al(OH)3 → Na3[Al(OH)6] с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
Al Oh 3 Hno3 EDUCA
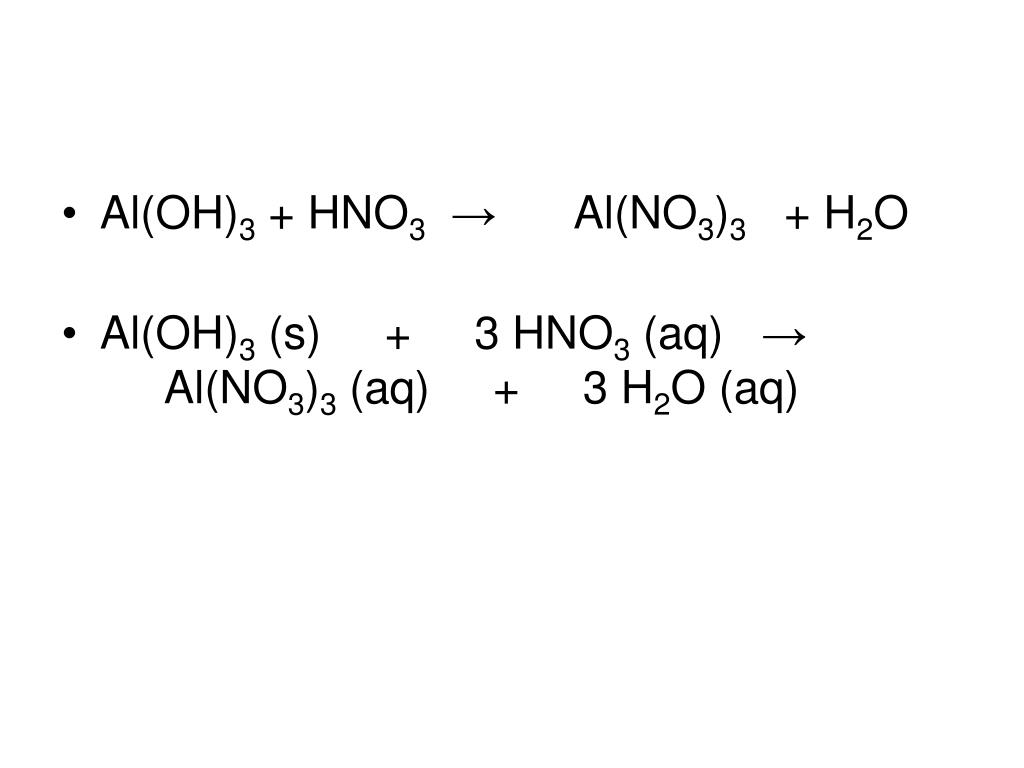
Калькулятор химических реакций. Воспользуйтесь калькулятором ниже для решения уравнений и вычисления типа реакции (инструкции). Химическое уравнение (H2O = H + O) Уравнять реакцию .
Напишите уравнения реакций Al(OH)3 AlCl3 Al(OH)3 Al2O3 (в ионном виде) Школьные

Geselle Гений (63456) 8 лет назад. Если это взаимодействие в растворе, то уравнение имеет вид: Al (OH)3 + NaOH = Na [Al (OH)4] В краткой ионной форме (образование комплексного иона): Al (OH)3 + OH (-) = [Al (OH)4] (-) Но если это.
уравнение в свете тед. AL2(SO4)3+NAOH= FE(OH)3+HCL= AL(OH)3+HNO3= NA2CO3+HNO3= Школьные

1 ответ. Xumuk ответил 7 лет назад. В результате взаимодействия гидроксида алюминия с азотной кислотой (Al (OH)3 + HNO3 = ?) происходит образование средней соли - нитрата алюминия и воды (обмен.
Пожалуйста !!!!!!!!!Химия сокращённое ,молекулярное и полное ионное уравнение Школьные

Al(OH)3+HCL-AlCL3+H2O составить ионное и молекулярное уравнение - ответ на этот и другие вопросы получите онлайн на сайте Uchi.ru
100 баллов решите.. Допиши уравнения химических реакций, характеризующие химические свойства

AlCL3(изб) +3NAOH= AL(OH)3+3NACL ионное уравнение - ответ на этот и другие вопросы получите онлайн на сайте Uchi.ru. Al +3 + 3Cl-+ 3Na + + 3OH-→ Al(OH) 3 ↓ + 3Na + + 3Cl - (полный ионный вид уравнения, Al(OH) 3 - нерастворимое.
Alalcl3al(oh)3al2o3и посложнее )) (на картинке ) составьте уравнения ) спасибо заранее

Al(OH)3+NaOH=Na[Al(OH)4] Можно ли составит ионное уравнение, если нет, то почему? Ответ 2.5/5 ( 2 оценки)
По краткому ионному уравнению составьте молекулярное и полное ионное уравнения Fe(3+)+3oh=Fe(OH

Какие продукты образуются в результате взаимодействия Al(OH)3 + NaOH = ? Надо записать молекулярное и ионное уравнение реакции, а также решить задачу. Вот условие: какая масса соли образуется при.
Напишите уравнение реакции в молекулярной и ионной формах Al(OH)3 + NaOH → Школьные

Химические Уравнения oнлайн! Послать. Расширенный поиск. Или Попробуйте случайную реакцию. Приложение для вычисления и дополнения продуктов реакции. Ионные и окислительно.
Cân bằng Al(OH)3 + NaOH = H2O + NaAlO2 (và phương trình Al(OH)3 + KOH)
Заниматься. Геля 5 лет назад. Na3 [Al (OH)6] вроде так. Спасибо 0. AL (OH)3 + NaOH = - ответ на этот и другие вопросы получите онлайн на сайте Uchi.ru.