Gases ideales

La constante de los gases, representada por el símbolo "R", es la constante de proporcionalidad de ley de los gases ideales. Ésta última es una ecuación matemática que relaciona las cuatro variables que definen completamente el estado de un gas ideal, esto es, la presión, el volumen, la temperatura y el número de moles.Además, esta ley es una combinación de todas las leyes de los.
Ecuacion general gases ideales
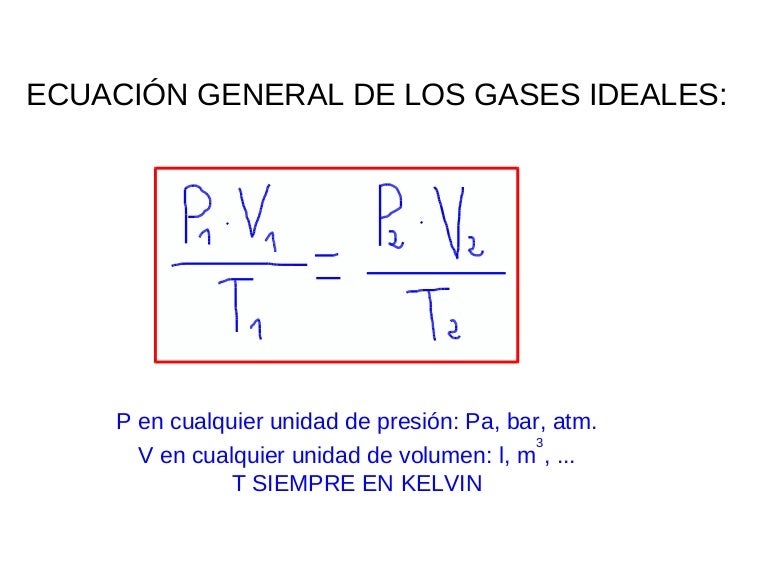
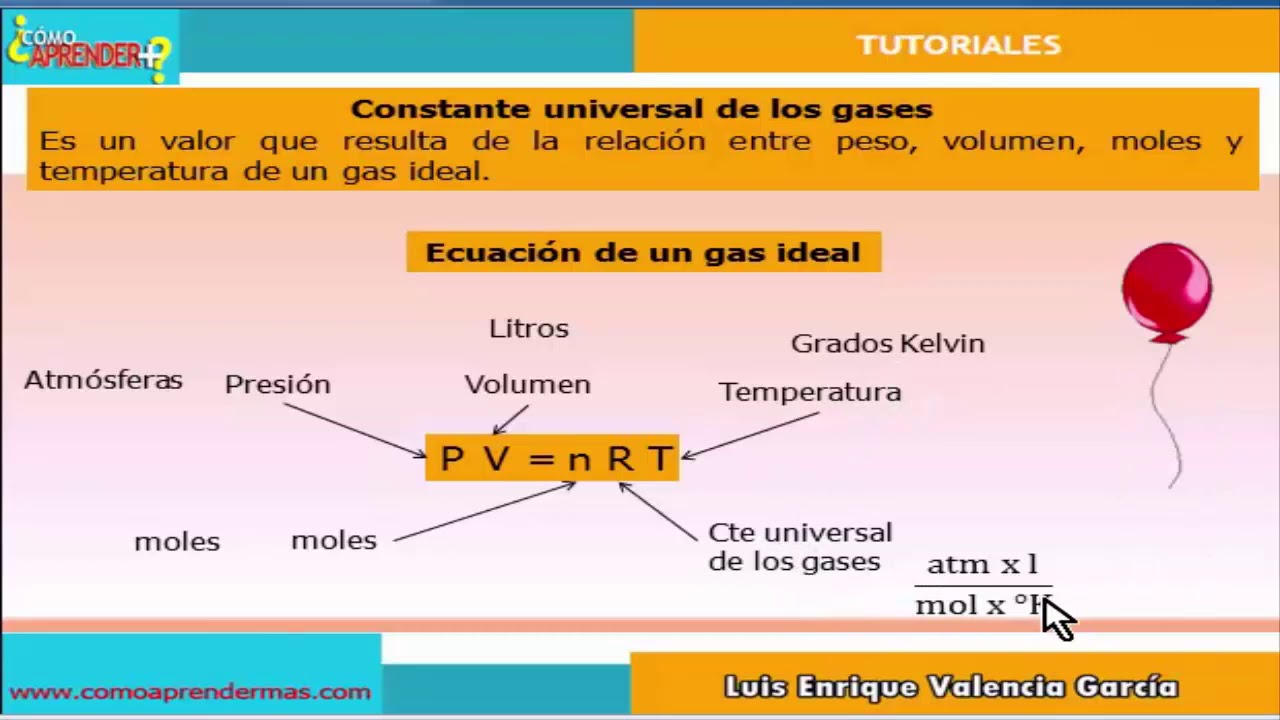
La presión, P , la temperatura, T , y el volumen, V , de un gas ideal, están relacionados por una simple fórmula llamada la ley del gas ideal. La simplicidad de esta relación es una razón por la que típicamente tratamos a los gases como ideales, a menos que haya una buena justificación para no hacerlo. P V = n R T.
🎈 Ecuación universal de los gases ideales YouTube

En esta clase se explica como hallar la constante R de los gases ideales para cualquier unidad de presión, volumen y temperatura para sistema internacional.
Constante Universal de los Gases

La constante universal de los gases es una constante física que aparece en muchas ecuaciones, particularmente en la ley de gas ideal PV = nRT . Se puede interpretar como la relación entre la escalas de energía y temperatura. Está definida como R ≡ N. k. , donde N A es la constante. B de Avogadro y k es la constante de Boltzmann.
Constante universal de los gasesecuación de estadoejercicio 3 YouTube

La ley de presión parcial de Dalton dice que la presión total de una mezcla de gases es igual a la suma de las presiones parciales de los gases que componen la mezcla: P Total = P gas 1 + P gas 2 + P gas 3.. La ley de Dalton también se puede expresar usando la fracción molar de un gas, x. . : P gas 1 = x 1 P Total.
Ecuación General de los Gases Ideales YouTube

Ecuación de la ley de los gases ideales. Todas las propiedades de un gas ideal se resumen en una fórmula: p V = n R T pV = nRT. donde: V V - volumen del gas, medido en m 3. n n - cantidad de sustancia, medida en moles. R R - constante de los gases ideales. T T - temperatura del gas, medida en kelvin.
Ecuación de los gases Academia Alfa10

La ley de los gases ideales (PV = nRT) relaciona las propiedades macroscópicas de los gases ideales. Un gas ideal es un gas en el que las partículas (a) no se atraen ni se repelen mutuamente y (b) no ocupan espacio (no tienen volumen). Ningún gas es verdaderamente ideal, pero la ley de los gases ideales sí proporciona una buena.
Valor numérico das constantes geral dos gases Físicoquímica II
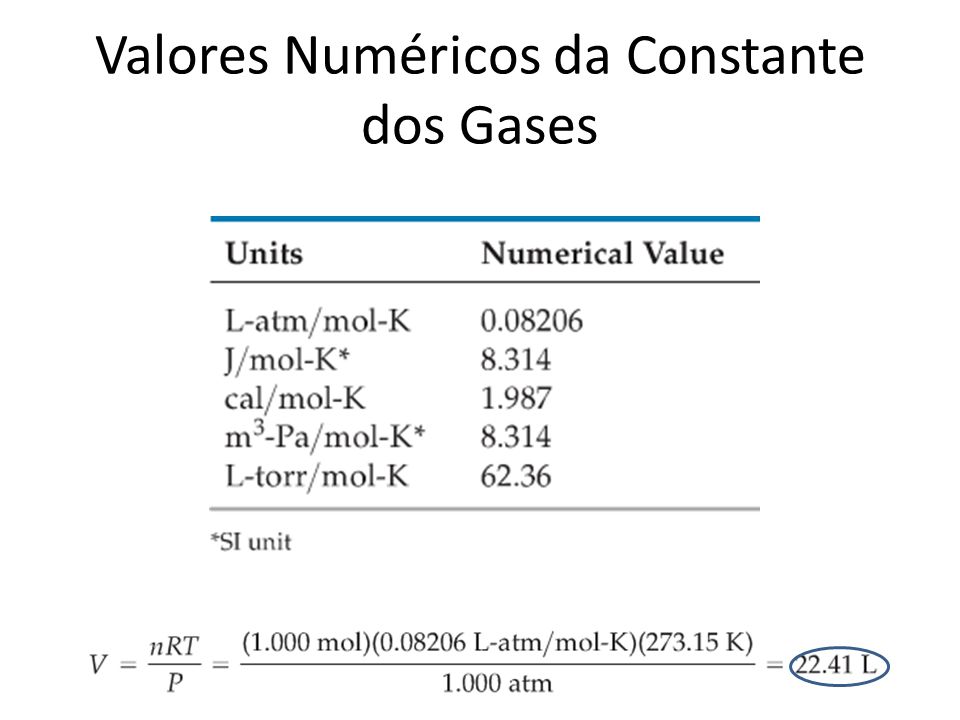
Mientras n es el número de moles, R la constante universal de los gases, y T la temperatura expresada en Kelvin (K). La expresión más usada en los gases para R equivale a 0,08206 L·atm·K-1 ·mol-1. Aunque la unidad SI para la constante de los gases tiene un valor de 8,3145 J·mol-1 ·K-1. Ambas son válidas siempre y cuando se tenga.
Gases Ideales Definiciones, características, ejercicios y más
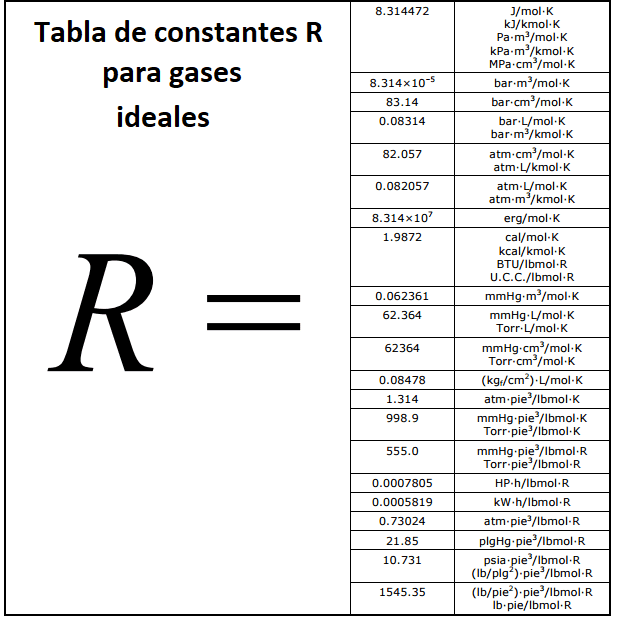
La constante universal de los gases ideales, constante de los gases o constante molar de los gases 1 2 3 es una constante física, más concretamente termodinámica, que establecida inicialmente en relación con variables del estado gaseoso: volumen, presión, temperatura y cantidad de sustancia, ha devenido en una constante de gran importancia.
Ecuación del Gas Ideal YouTube

En su forma más particular la constante se emplea en la relación de la cantidad de materia en un gas ideal, medida en número de moles (n), con la presión (P), el volumen (V) y la temperatura (T), a través de la ecuación de estado de los gases ideales . El modelo del gas ideal asume que el volumen de la molécula es cero y las partículas no interactúan entre si.
PPT Leyes de los Gases PowerPoint Presentation, free download ID4792257
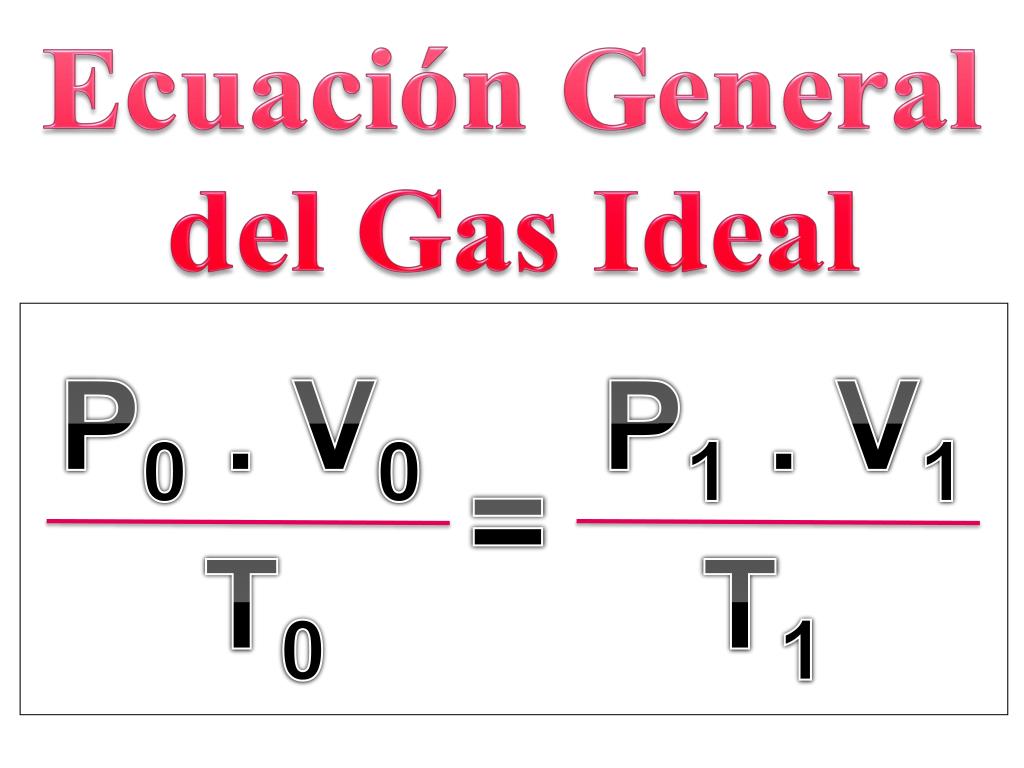
Donde, R es la constante de los gases ideales y su valor es 0.08205 [L·atm·mol-1·K-1], lo cual implica que el volumen se debe trabajar en litros, la presión en atmósferas, la temperatura en Kelvin y la . 2 cantidad de gas en moles. A dicha expresión, se le llama ecuación de estado del gas ideal porque
Constante universal de los gasesEcuación de estado YouTube
La constante de gas universal (R) es 8.3144598 J/ (mol·K). [1] La constante de gas (también conocido como el molar, universal, o constante de gas ideal, se representa con el símbolo R o R) es un constante física cual es destacado en muchos ecuaciónes fundamental en las ciencias naturales, por ejemplo la ley de los gases ideales y la.
Ecuación de estado de los gases ideales YouTube

La ecuación de los gases ideales contiene cinco términos, la constante de los gases R y las propiedades variables P, V, n y T. La especificación de cualquiera de estos términos permitirá el uso de la ley de los gases ideales para calcular el quinto término, como se demuestra en los siguientes ejercicios de ejemplo.
IdealGas Equation The constant of proportionality is R

The molar gas constant (also known as the gas constant, universal gas constant, or ideal gas constant) is denoted by the symbol R or R.It is the molar equivalent to the Boltzmann constant, expressed in units of energy per temperature increment per amount of substance, rather than energy per temperature increment per particle.The constant is also a combination of the constants from Boyle's law.
Gases ideales
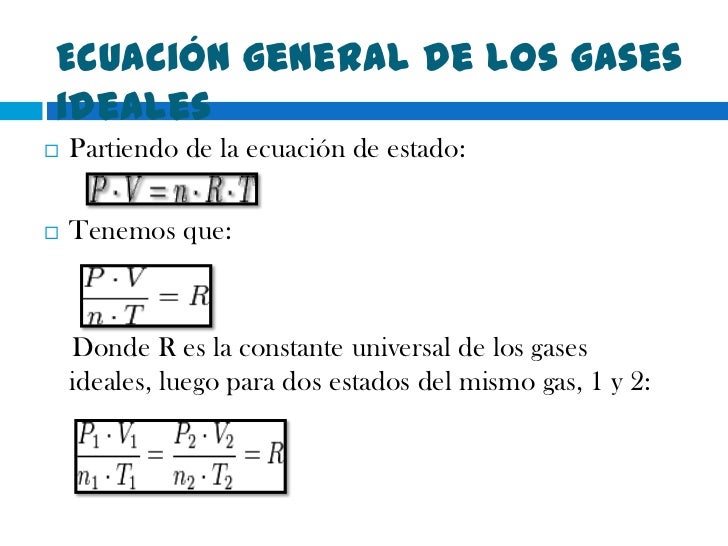
Ecuación de los gases ideales. Ejemplo 4. Ejemplo resuelto: Relacionar la estequiometría de reacción y la ley de los gases ideales. es igual a 273 grados kelvin esto está en kelvin atmósfera y el volumen lo queremos en litros entonces cuál es la constante r que usaremos vamos a ver si trabajamos con atmósferas y queremos el volumen en.
Ecuación del gas ideal (Ejemplo paso a paso y valores de R) YouTube

Figura 1. El valor de la constante de los gases en diferentes sistemas de unidades. Fuente: F. Zapata. Donde P es la presión, V es el volumen, T la temperatura, n la cantidad de moles presentes en una porción de gas ideal y R es precisamente la constante de los gases. Su valor, determinado experimentalmente es de 0.0821 L ∙ atm/K ∙ mol.